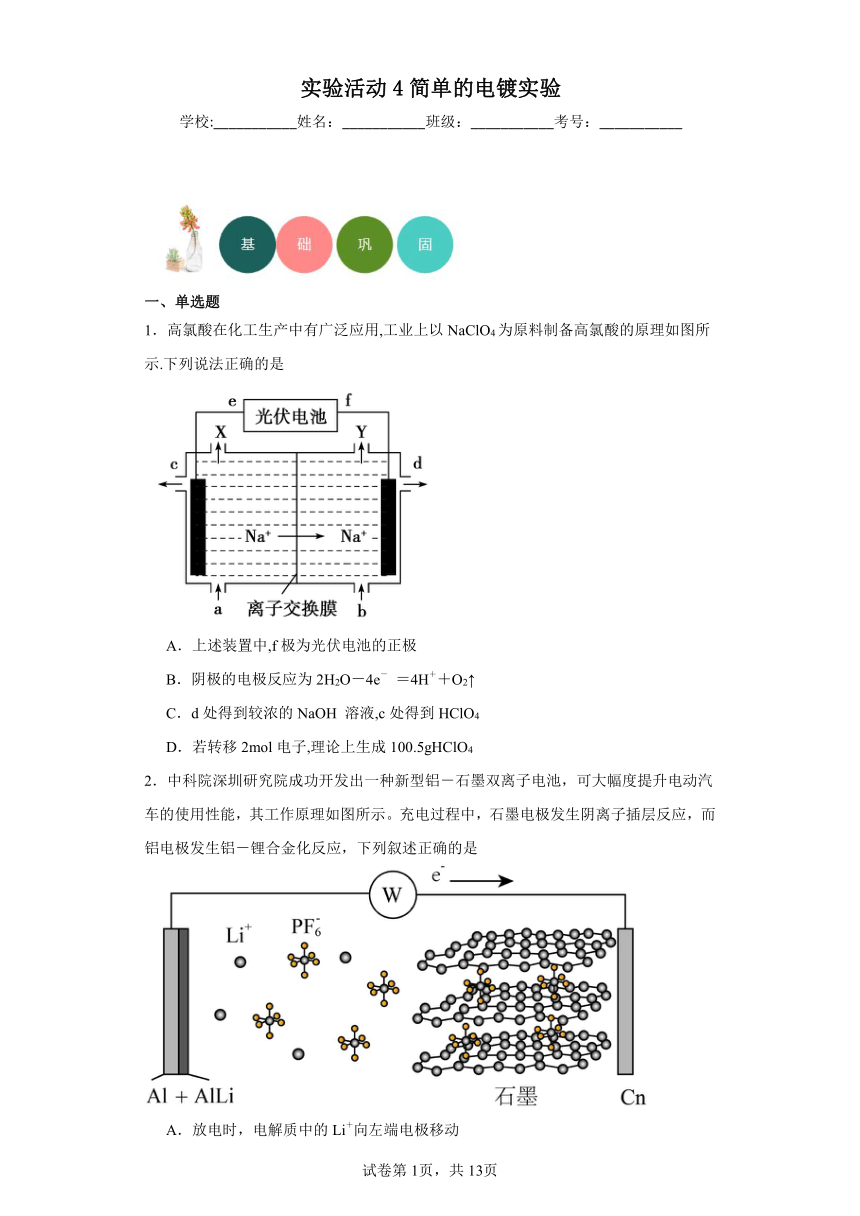
实验活动4简单的电镀实验 学校:_____姓名:_____班级:_____考号:_____ 一、单选题 1.高氯酸在化工生产中有广泛应用,工业上以NaClO4为原料制备高氯酸的原理如图所示.下列说法正确的是 A.上述装置中,f极为光伏电池的正极 B.阴极的电极反应为2H2O-4e- =4H++O2↑ C.d处得到较浓的NaOH 溶液,c处得到HClO4 D.若转移2mol电子,理论上生成100.5gHClO4 2.中科院深圳研究院成功开发出一种新型铝-石墨双离子电池,可大幅度提升电动汽车的使用性能,其工作原理如图所示。充电过程中,石墨电极发生阴离子插层反应,而铝电极发生铝-锂合金化反应,下列叙述正确的是 A.放电时,电解质中的Li+向左端电极移动 B.充电时,与外加电源负极相连一端电极反应为:AlLi-e-=Li++Al C.放电时,正极反应式为Cn(PF6)+e-=PF6-+Cn D.充电时,若转移0.2mol电子,则铝电极上增重5.4g 3.某同学组装如图所示电化学装置,电极I为Zn,其它电极均为Cu。下列说法错误的是 A.电极I发生氧化反应 B.相同的时间内,电极Ⅱ与Ⅳ质量变化相同 C.电极III的电极反应:4OH――4e-=2H2O+O2↑ D.电流方向:电极Ⅳ→→电极I 4.高锰酸钾也可以通过电解法制备,装置如图所示。下列说法正确的是( ) A.a是电源的负极 B.离子交换膜是阴离子交换膜 C.转移电子1 mol阴极生成气体11.2 L D.转移电子2 mol,生成KMnO4 2 mol 5.储氢作为氢能利用的关键技术,是当前关注的热点之一。一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物).下列说法错误的是( ) 已知:电流效率(η=×100%) A.电源B为正极 B.导线中电子移动方向为A→D C.电极D反应式为C6H6+6H++6e-=C6H12 D.该储氢装置的电流效率η=24.3% 6.三氧化二镍(Ni2O3)可用于制造高能电池元件。电解法制备过程如下:用NaOH 溶液将NiCl2溶液的pH调至7.5(该pH下溶液中的Ni2+不沉淀),加入适量硫酸钠固体后进行电解。电解过程中产生的Cl2(不考虑Cl2的逸出)在弱碱性条件下生成ClO﹣,ClO﹣再把二价镍(可简单写成Ni2+)氧化为Ni3+,再将Ni3+经一系列反应后转化为Ni2O3,电解装置如图所示。下列说法不正确的是( ) A.加入适量硫酸钠的作用是增加离子浓度,增强溶液的导电能力 B.电解过程中阴、阳两极附近溶液的pH均升高 C.当有1mol Ni2+氧化为Ni3+时,外电路中通过的电子数目为1NA,通过阳离子交换膜的Na+数目为1NA D.反应前后b池中Cl- 浓度几乎不变 7.用惰性电极电解下列各组中的三种溶液,电解过程中,溶液中c(H+ )依次为升高、不变、降低的是( ) A.CuSO4、Na2SO4、KCl B.AgNO3、CuCl2、Cu(NO3)2 C.CaCl2、KOH、NaNO3 D.HCl、HNO3、K2SO4 8.在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是 A.阴、阳两极生成的气体的物质的量之比是1︰2 B.X是电源的负极 C.阴极的反应式是:H2O+2e-=H2+O2- CO2+2e-=CO+O2- D.总反应可表示为:H2O+CO2H2+CO+O2 9.下列有关CuSO4溶液的叙述中正确的是 A.该溶液呈碱性 B.它与H2S反应的离子方程式为:Cu2++S2-=CuS↓ C.用惰性电极电解该溶液时,阳极产生铜单质 D.在溶液中:2c (Cu2+) +c (H+)=2c(SO42-) +c(OH-) 10.某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置,使浆液分离成固体混合物和含铬元素溶液,并回收利用。用惰性电极电解时,下列说法正确的是: A.a极产生氧气,b极产生氢气 B.a电极区溶液pH值减小 C.含铬微粒主要以Cr2O72-形式在b极区聚集 D.CrO42-能从浆液中分离出来向a极区迁移 二、填空题 11.(1)在用惰性电极电解水制取H2 ... ...
~~ 您好,已阅读到文档的结尾了 ~~