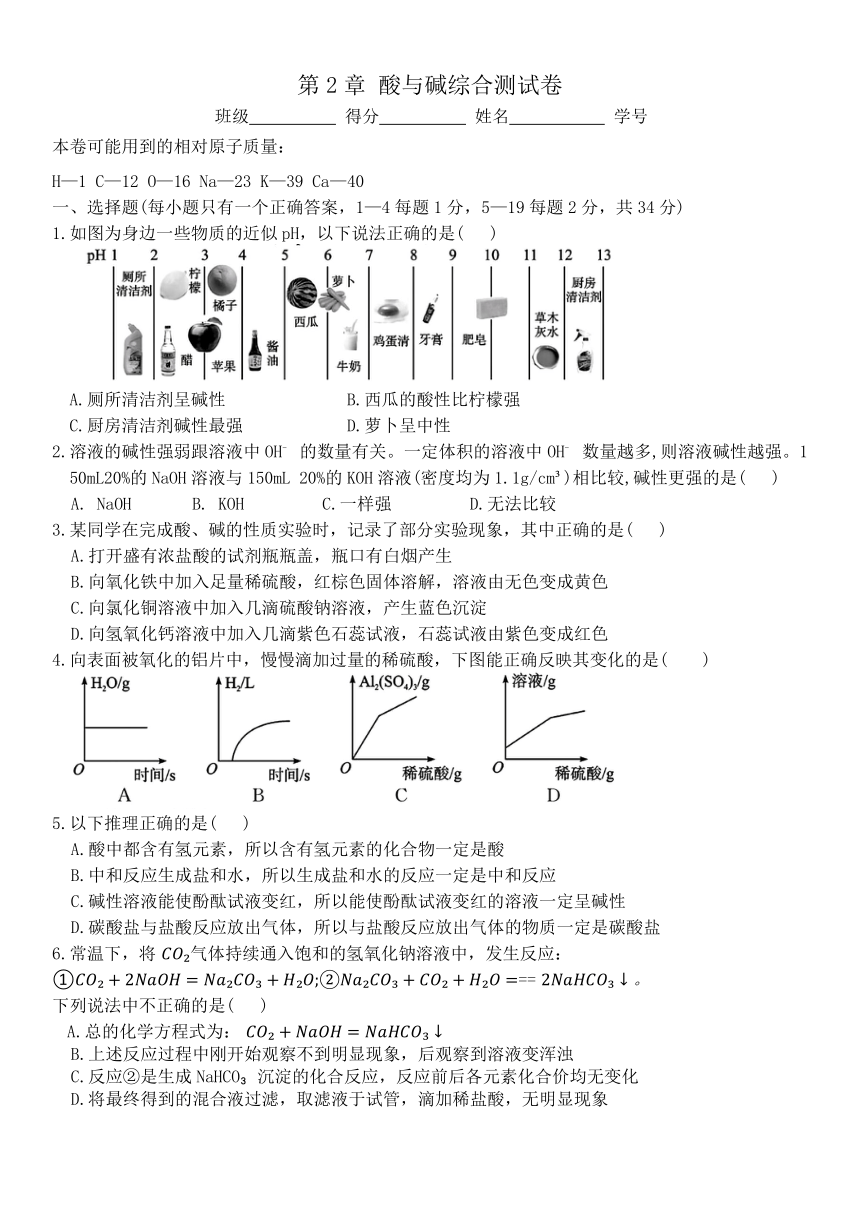
第2章 酸与碱综合测试卷 班级 得分 姓名 学号 本卷可能用到的相对原子质量: H—1 C—12 O—16 Na—23 K—39 Ca—40 一、选择题(每小题只有一个正确答案,1—4每题1分,5—19每题2分,共34分) 1.如图为身边一些物质的近似pH,以下说法正确的是( ) A.厕所清洁剂呈碱性 B.西瓜的酸性比柠檬强 C.厨房清洁剂碱性最强 D.萝卜呈中性 2.溶液的碱性强弱跟溶液中OH 的数量有关。一定体积的溶液中OH 数量越多,则溶液碱性越强。150mL20%的NaOH溶液与150mL 20%的KOH溶液(密度均为1.1g/cm )相比较,碱性更强的是( ) A. NaOH B. KOH C.一样强 D.无法比较 3.某同学在完成酸、碱的性质实验时,记录了部分实验现象,其中正确的是( ) A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口有白烟产生 B.向氧化铁中加入足量稀硫酸,红棕色固体溶解,溶液由无色变成黄色 C.向氯化铜溶液中加入几滴硫酸钠溶液,产生蓝色沉淀 D.向氢氧化钙溶液中加入几滴紫色石蕊试液,石蕊试液由紫色变成红色 4.向表面被氧化的铝片中,慢慢滴加过量的稀硫酸,下图能正确反映其变化的是( ) 5.以下推理正确的是( ) A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸 B.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 C.碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性 D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 6.常温下,将 气体持续通入饱和的氢氧化钠溶液中,发生反应: ①== 下列说法中不正确的是( ) A.总的化学方程式为: B.上述反应过程中刚开始观察不到明显现象,后观察到溶液变浑浊 C.反应②是生成NaHCO 沉淀的化合反应,反应前后各元素化合价均无变化 D.将最终得到的混合液过滤,取滤液于试管,滴加稀盐酸,无明显现象 7.醋是家庭中不可缺少的调味品之一,同时醋还具有较强的杀灭细菌、抑制病毒的作用。另外,醋可使胃中酸性增强,促进食欲,帮助消化,对于胃酸较少的人而言更是一剂良药。醋的主要成分是醋酸,其化学式为 下列有关叙述中错误的是( ) A.醋酸的水溶液呈酸性,是因为醋酸能解离出 H B.醋酸能与碳酸钠溶液反应生成醋酸钠、二氧化碳和水,该反应为中和反应 C.用醋酸可以洗去铝制品的污垢,还可除去暖壶、水壶中的水垢 D.胃酸过多的病人可服用含小苏打的药剂降低胃酸 8.下列实验所残留的物质可以用稀盐酸除掉的是( ) ①二氧化碳通入澄清石灰水后附在试管壁上的白色物质 ②氢氧化钠溶液滴入盛有氯化铁溶液的试管上附着的红褐色物质 ③稀硫酸溶液滴入盛有硝酸钡溶液的试管上附着的白色物质 ④碳酸钠溶液滴入盛有氯化钡溶液的试管上附着的白色物质 A.③④ B.②③ C.①③ D.①②④ 9. 在实验课上进行了“魔壶”的实验。将“魔壶”中盛有的液体依次倒入两个分别盛有不同溶液的的烧杯中,现象如表,下列有关说法正确的是 ( ) “魔壶”内盛有的液体 烧杯1中形成的“饮料” 烧杯 2中形成的“饮料” 稀硫酸 “牛奶” “雪碧” A.此实验用的“魔壶”能用铁制的 B.烧杯1中盛有的溶液一定是 C.烧杯2中得到“雪碧”饮料可能的原因是生成CO2 D.若将“魔壶”中的溶液改为稀硝酸溶液实验现象相同 10.下列物质中,都能跟稀硫酸、稀盐酸发生反应且反应中表现了“酸的通性”的组合是( ) ①金属锌 ②碳酸钠 ③氢氧化钙 ④氯化钡溶液 A.①②③ B.①③④ C.②③④ D.①②③④ 11.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下。由此分析下列说法正确的是( ) A.反应前后阴、阳离子的总数目不变 B.反应前后溶剂质量不变 C.反应后溶液呈中性 D.反应前后元素种类发生了变化 12.只含一种杂质的硫酸溶液 M,加入足量的氢氧化钡溶液后,再加足量的稀盐酸,过程如图所示。下列判断:①M中一定不含有碳酸钠;② ... ...
~~ 您好,已阅读到文档的结尾了 ~~