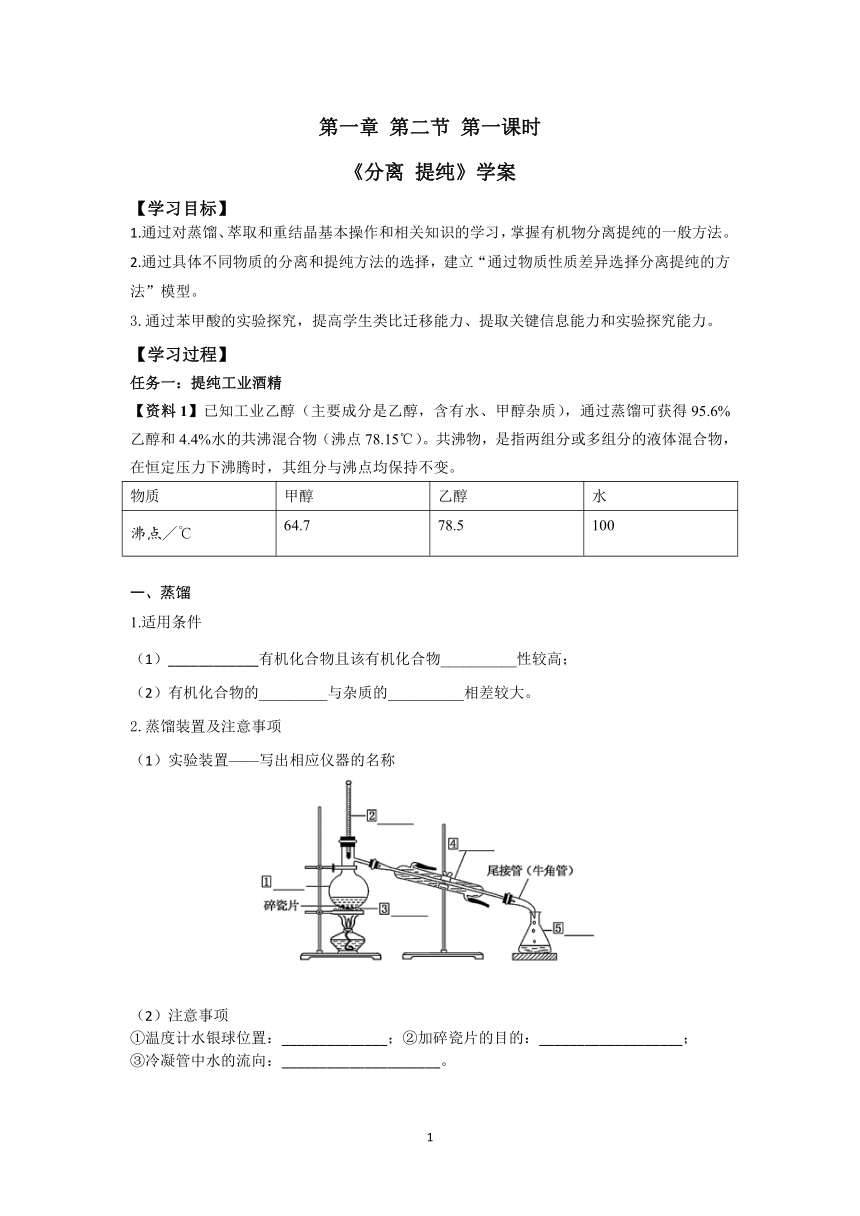
第一章 第二节 第一课时 《分离 提纯》学案 【学习目标】 通过对蒸馏、萃取和重结晶基本操作和相关知识的学习,掌握有机物分离提纯的一般方法。 通过具体不同物质的分离和提纯方法的选择,建立“通过物质性质差异选择分离提纯的方法”模型。 通过苯甲酸的实验探究,提高学生类比迁移能力、提取关键信息能力和实验探究能力。 【学习过程】 任务一:提纯工业酒精 【资料1】已知工业乙醇(主要成分是乙醇,含有水、甲醇杂质),通过蒸馏可获得95.6%乙醇和4.4%水的共沸混合物(沸点78.15℃)。共沸物,是指两组分或多组分的液体混合物,在恒定压力下沸腾时,其组分与沸点均保持不变。 物质 甲醇 乙醇 水 沸点/℃ 64.7 78.5 100 一、蒸馏 1.适用条件 (1)_____有机化合物且该有机化合物_____性较高; (2)有机化合物的_____与杂质的_____相差较大。 2.蒸馏装置及注意事项 (1)实验装置———写出相应仪器的名称 (2)注意事项 ①温度计水银球位置:_____;②加碎瓷片的目的:_____; ③冷凝管中水的流向:_____。 【思考】1.如何获得无水乙醇? 2.固液混合物分离为什么不用过滤而用蒸馏呢? 任务二:从碘水中提取碘单质 【资料2】 二、萃取 类型 液-液萃取:利用待分离组分在两种_____的溶剂中的_____不同,将其从一种溶剂转移到另一种溶剂的过程。 固-液萃取:用_____从_____物质中溶解出待分离组分的过程 装置和仪器 萃取剂 对萃取剂的要求: ①萃取剂与原溶剂_____; ②溶质在萃取剂中的溶解度_____在原溶剂中的溶解度; ③萃取剂与原溶液中的成分不反应 常用萃取剂:_____ 分液 定义 将萃取后的两层液体分开的操作 操作 加入萃取剂后充分振荡,静置分层,然后打开分液漏斗上方的玻璃塞和下方的活塞将两层液体分离,下层液体从_____流出,并及时关闭活塞,上层液体从_____倒出 【思考】 1.碘易溶于酒精,能否用酒精将碘水中的碘萃取出来?为什么? 2.分液后应如何分离碘的四氯化碳有机溶液? (已知:四氯化碳沸点:76.8 ℃ 碘单质沸点:184.35 ℃) 任务三:提纯苯甲酸 【资料3】苯甲酸可用作食品防腐剂,纯净的苯甲酸为无色结晶,其结构可表示为 ,熔点122℃,沸点249℃,苯甲酸微溶于水,易溶于乙醇等有机溶剂。苯甲酸、氯化钠在水中的溶解度如下: 温度 25℃ 50℃ 95℃ 苯甲酸 0.34g 0.85g 6.8g NaCl 36.0 37.0 39.1 【思考】某粗苯甲酸样品中含有少量氯化钠和泥沙,如何提纯苯甲酸? 三、重结晶 【思考】 1.结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤? 2.溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么? 3.实验操作中多次用到了玻璃棒,分别起到了哪些作用? 如何检验提纯后的苯甲酸中氯化钠已被除净? 任务四:总结归纳 【学习效果】 一、单项选择题I 1.下列说法不正确的是( ) A.蒸馏是分离、提纯液态有机化合物的常用方法 B.重结晶的首要工作是选择适当的溶剂 C.萃取包括液-液萃取和固-液萃取 D.研究有机化合物可首先进行元素定量分析,再分离、提纯 2.下列操作中选择的仪器正确的是( ) ①分离汽油和氯化钠溶液 ②从含Fe3+的自来水中得到蒸馏水 ③分离氯化钾和二氧化锰混合物 ④从食盐水中提取溶质 A.①—丁 ②—丙 ③—甲 ④—乙 B.①—乙 ②—丙 ③—甲 ④—丁 C.①—丁 ②—丙 ③—乙 ④—甲 D.①—丙 ②—乙 ③—丁 ④—甲 3.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是 A.在组装蒸馏装置时,温度计的水银球应伸入液面下 B.用96%的工业酒精制取无水乙醇,可采用直接蒸馏的方法 C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水 D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤 4.下列实验中,所采取的分 ... ...
~~ 您好,已阅读到文档的结尾了 ~~