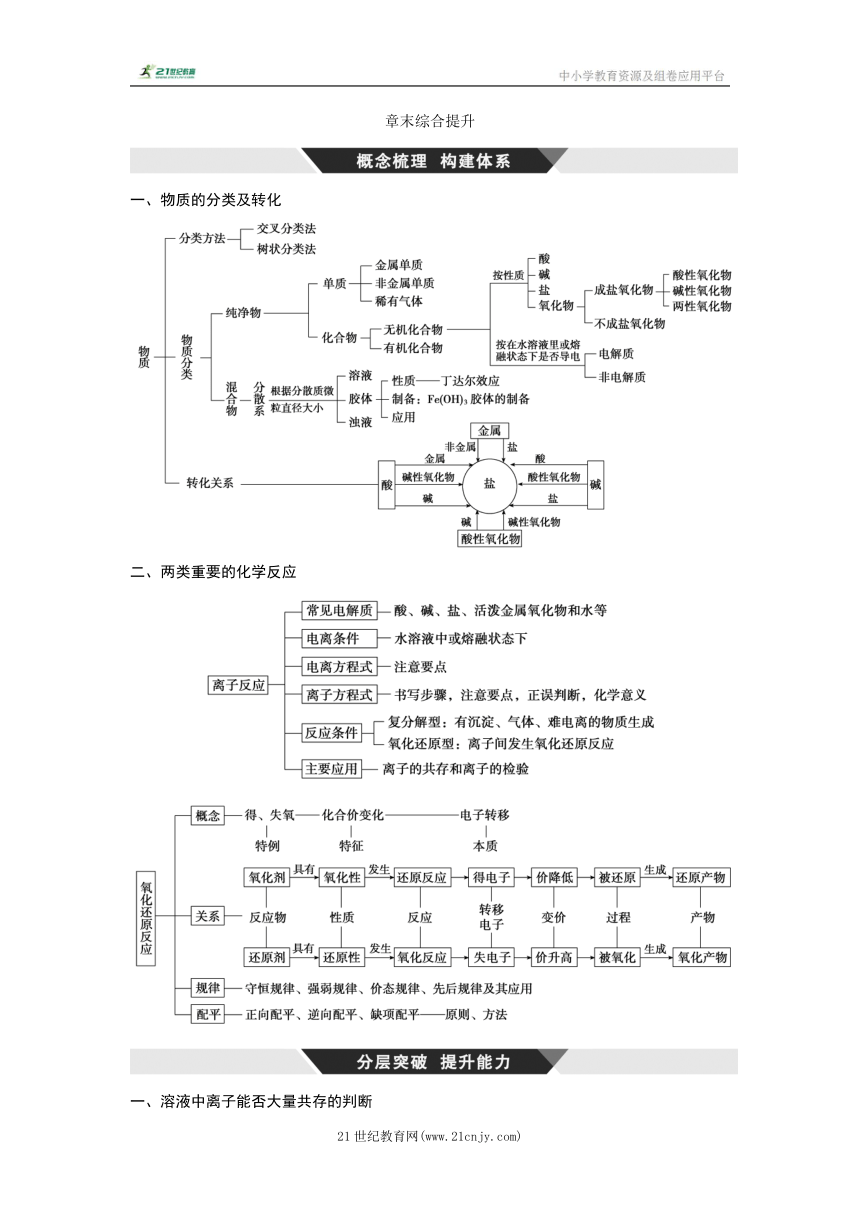
章末综合提升 一、物质的分类及转化 二、两类重要的化学反应 一、溶液中离子能否大量共存的判断 1.溶液中离子能否大量共存的判断方法 判断溶液中的离子能否大量共存,事实上是看离子之间能否反应,若反应,则不能大量共存;若不反应,则能大量共存。 2.离子不能大量共存的五种情况 (1)离子间因生成难溶于水(或微溶于水)的物质而不能大量共存 ①OH-分别与Fe2+、Fe3+、Mg2+、Cu2+、Al3+、Ag+、Ca2+在溶液中不能大量共存; ②Ba2+(或Ca2+)分别与SO、SO、CO、SiO、PO在溶液中不能大量共存; ③Ag+分别与Cl-、Br-、I-、CO、SO等在溶液中不能大量共存; ④Cu2+(或Fe2+)与S2-在溶液中不能大量共存。 (2)离子间因生成气体而不能大量共存 H+分别与CO、HCO、S2-、HS-、SO、HSO在溶液中不能大量共存。 (3)多元弱酸的酸式酸根(如HCO、HSO、HS-等)在强酸或强碱性溶液中均不能大量共存 例如:HCO+H+===CO2↑+H2O;HCO+OH-===CO+H2O。 (4)离子间因发生氧化还原反应而不能大量共存 例如:S2-、I-、Fe2+等还原性离子与NO(H+)、MnO(H+)、ClO-等氧化性离子在溶液中不能大量共存。 (5)“无色透明”溶液不能大量存在有色离子,例如: Cu2+ Fe3+ Fe2+ MnO | | | | 蓝色 棕黄色 浅绿色 紫红色 针对练1.(2023 海淀区第五十七中学高一月考)下列各组离子能在水溶液中大量共存的是( ) A.H+、Na+、SO、Cl- B.K+、Cu2+、Cl-、OH- C.Mg2+、Ba2+、CO、SO D.Ag+、Ca2+、Cl-、NO 答案:A 解析:H+、Na+、SO、Cl-相互之间不发生反应,可以大量共存,A符合题意;Cu2+与OH-反应生成Cu(OH)2沉淀,不能大量共存,B不符合题意;Mg2+、Ba2+与CO可以生成MgCO3、BaCO3沉淀,Ba2+与SO反应生成BaSO4沉淀,不能大量共存,C不符合题意;Ag+与Cl-生成AgCl沉淀,不能大量共存,D不符合题意。 针对练2.(2023 丰城市东煌学校高一月考)下列各组离子,能在溶液中大量共存的是( ) A.Ag+、K+、I-、NO B.H+、Na+、CO、MnO C.H+、Mg2+、Cl-、SO D.Ba2+、Al3+、Cl-、SO 答案:C 解析:银离子和碘离子生成碘化银沉淀,故A错误;氢离子和碳酸根离子生成二氧化碳气体,故B错误;四种离子相互之间不反应,能共存,故C正确;Ba2+与SO生成硫酸钡沉淀,不能大量共存,故D错误。 针对练3.下列各组离子在指定溶液中一定能大量共存的是( ) A.碳酸钠溶液中:NH、Ca2+、Cl-、NO B.能使酚酞变红的溶液中:Na+、Ba2+、Cl-、NO C.含有大量HCO的溶液:Na+、NO、Cl-、H+ D.无色透明溶液中:K+、I-、SO、MnO 答案:B 解析:Ca2+与碳酸钠溶液中的碳酸根离子反应生成碳酸钙,在溶液中不能大量共存,故A不符合题意;能使酚酞变红的溶液中存在大量氢氧根离子,Na+、Ba2+、Cl-、NO之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B符合题意;HCO、H+之间发生反应生成二氧化碳和水,在溶液中不能大量共存,故C不符合题意;MnO为紫红色,为有色离子,I-、MnO之间发生氧化还原反应,在溶液中不能大量共存,故D不符合题意。 二、信息型氧化还原反应方程式的书写 一判:根据题给信息,联想所学知识,判断主要的反应物、生成物。 若反应物、生成物中主要元素化合价不一致的,要考虑是否为氧化还原反应,就要写出氧化剂、还原剂、氧化产物、还原产物。 二平:根据质量守恒定律和氧化还原反应规律配平主要物质的化学计量数。 三补:根据溶液的介质条件以及电荷守恒补足反应物或生成物,一般酸性环境可以消耗或生成酸,碱性环境可以消耗或生成碱。 针对练4.(1)某反应的反应物与生成物有K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性:K2Cr2O7>Cl2 ... ...
~~ 您好,已阅读到文档的结尾了 ~~