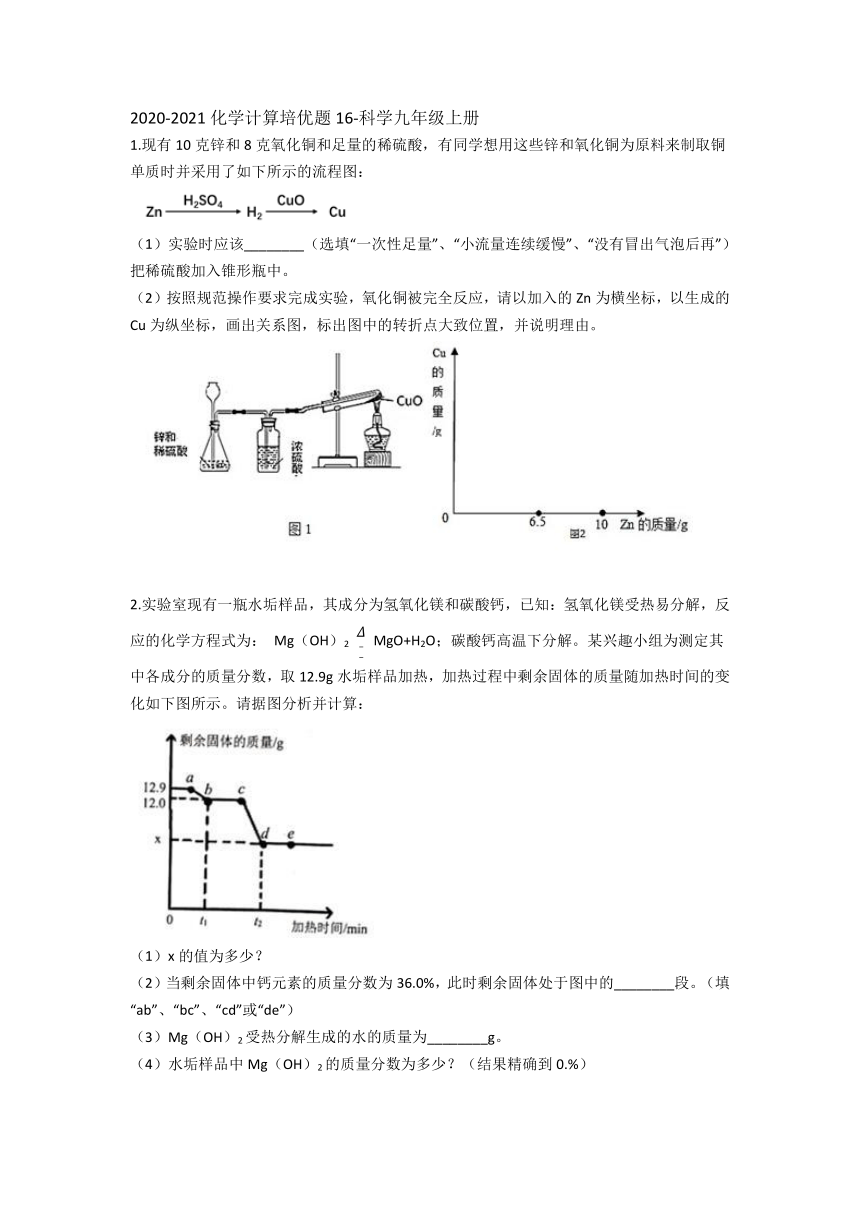
2020-2021化学计算培优题16-科学九年级上册 1.现有10克锌和8克氧化铜和足量的稀硫酸,有同学想用这些锌和氧化铜为原料来制取铜单质时并采用了如下所示的流程图: (1)实验时应该_____(选填“一次性足量”、“小流量连续缓慢”、“没有冒出气泡后再”)把稀硫酸加入锥形瓶中。 (2)按照规范操作要求完成实验,氧化铜被完全反应,请以加入的Zn为横坐标,以生成的Cu为纵坐标,画出关系图,标出图中的转折点大致位置,并说明理由。 2.实验室现有一瓶水垢样品,其成分为氢氧化镁和碳酸钙,已知:氢氧化镁受热易分解,反应的化学方程式为: Mg(OH)2 Δ__ MgO+H2O;碳酸钙高温下分解。某兴趣小组为测定其中各成分的质量分数,取12.9g水垢样品加热,加热过程中剩余固体的质量随加热时间的变化如下图所示。请据图分析并计算: (1)x的值为多少? (2)当剩余固体中钙元素的质量分数为36.0%,此时剩余固体处于图中的_____段。(填“ab”、“bc”、“cd”或“de”) (3)Mg(OH)2受热分解生成的水的质量为_____g。 (4)水垢样品中Mg(OH)2的质量分数为多少?(结果精确到0.%) 3.?菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示 已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O?? ②菱铁矿中杂质不参加反应,且难溶于水. 请计算: (1)20.0g菱铁矿中FeCO3的质量为_____? g. (2)列式计算所用稀硫酸的溶质质量分数(结果准确到0.1%) 4.将40g稀盐酸逐滴加入20g溶质质量分数为4%的氢氧化钠溶液中,边滴边搅拌。随着稀盐酸的滴加,溶液的pH变化如图甲所示,溶液的温度变化如图乙所示(不考虑反应过程中热量损失)。试分析: (1)图乙从A到B过程中,溶液pH逐渐_____(选填“增大”或“减小”)。 (2)图乙表示酸碱恰好完全反应的点是_____。 (3)计算稀盐酸中溶质的质量分数。 5.某校初三某班学生去春游,带回了几小块石灰石样品,为了检测样品中碳酸钙的含量.甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如表: 甲同学 乙同学 丙同学 丁同学 所取石灰石样品质量(g) 10.0 10.0 10.0 10.0 ?? 加入盐酸的质量(g) 10.0 20.0 30.0 40.0 ?? 烧杯中剩余物质的总质量(g) 19.0 28.0 37.0 46.7 试问答: (1)四位同学里面,_____同学的实验样品完全反应;10.0g样品与_____?g盐酸恰好完全反应. (2)求样品中碳酸钙的质量分数(写出计算过程) (3)请在图中画出加入稀盐酸的质量与生成气体的质量的变化关系(标注必要的数值) 6.5G通讯需要大量光纤连接各种基站,在光纤的表面涂布Cu-Al合金层的金属涂层光纤是其中一种。为测定金属涂层光纤的Cu-Al合金层中铝的质量分数,小乐进行了相关实验,测得实验数据如表所示,则: 甲 乙 丙 加入Cu-Al合金层样品粉末的质量(g) 10 10 20 加入稀硫酸的质量(g) 100 50 50 烧杯中剩余物的质量(g) 109 59 69 (1)实验中Cu-Al合金层样品粉末与稀硫酸恰好完全反应的实验是_____?(选填“甲”“乙”或“丙”); (2)该Cu-Al合金层样品粉末中铝的质量分数为多少?(写出计算过程) 7.?某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓ (1)配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为_____?g. (2)计算MgSO4溶液中溶质的质量分数(列式计算). 8.石灰石是主要矿产品之一。某校研究性学习小组想要测量当地矿石中含CaCO3的质量分数。取一些矿石样 ... ...
~~ 您好,已阅读到文档的结尾了 ~~